高円寺南診療所では、人の居場所に着目したグローバルな医療の視点が必要と考え、家庭医学をはじめ産業医学(職場)、スポーツ医学、保養地医学などに関心を払ってきました。
しかし、国際社会に会って人の移動に着目した医療にも無関心であってはならないため、日本旅行医学会への入会手続き中です。
「旅行医学」とは、「人の移動の安全と快適性を高める医学」と定義されます。
日本旅行医学会のHPによると、日本旅行医学会の基本コンセプト は、統計的なアプローチを通して、科学的根拠のある具体的で分かりやすいメッセージを発信していこうということであると表明されています。
そこで、今回は日本旅行医学会のHPで解説している「感染症」のなかから、デング熱について引用してみることにしました。
病原体
デングウイルスは4種類の型があり、それぞれが免疫学的に関連しています。
このウイルスはプラス鎖のRNAウイルスで、フラビウイルス科のフラビウイルス属に属しており、デング熱とデング出血熱の両方を引き起こします。
無症候性感染もまたこのウイルスによって起こります。ある型のデングウイルスに感染すると、その型の再感染に対する免疫を生涯にわたり持続しますが、他の3つの型のウイルスに対する交叉防御免疫は長期間は持続しません(いずれの組合せの交叉免疫であっても2ヶ月以内)。
感染経路
人への感染は主としてウイルスに感染したネッタイシマカ(まれにヒトスジシマカやポリネシアヤブカ)に刺されて起こります。
雌の蚊がウイルス血症のヒトを刺してウイルスを宿すと、8~12日の外部潜伏期の経過後に感染状態となります。
感染した蚊はそれ以後はずっとデング熱ウイルスを感染させることができます(蚊の寿命は約1ヶ月)。
頻度は低くなりますが、輸血、内臓または骨髄移植、(針刺し、血液の粘膜接触等の)院内事故などによって汚染血液、内臓、その他の組織によりデング熱ウイルスに感染することもあります。
デング熱ウイルスが、感染した女性から子宮内の胎児へ、あるいは分娩の際に新生児へ垂直感染することもあります。
ヒトからヒトへの直接感染についての報告はありません。
発生地域
デング感染症は、アフリカ、南北アメリカ、カリブ海、地中海東岸、東南アジア、西太平洋の地域の100以上におよぶ諸国から報告されています(地図3-01、3-02)。
世界保健機構(WHO)の推定では、年間5000万件の発症があり、そのうちの50万件(1%)が入院を要するものとしています。
デング感染症の分布はマラリアと類似していますが、マラリアの場合と異なり、デング感染症は熱帯諸国の都市部や住宅地域での発生が多くみられます。
旅行をしようとする人はCDC(www.cdc.gov/dengue/travelOutbreaks/index.html)や WHO (http://www.who.int/topics/dengue/en/)のウェブサイトを調べて、旅行を計画している国がデング感染症の流行地であるかどうか、また現在流行中であるかどうかを判断することが求められます。
1980年以来、米国本土ではデング感染症の発生が何件か認められています。
その中には、テキサス南部のメキシコ国境沿いの地域での7件、2001年のハワイでの1件、2009年と2010年のフロリダ南部での2件の発生が含まれます。
米国南東部のいくつかの州では、ほぼ年中蚊が生息し、住民は感染を受けやすく、しかも国外からの旅行者や海外からの帰国者がウイルスを持ち込む機会が多くあります。
しかし、住宅設備(例えば、エアコンや防虫網)や生活様式を変えることによって、これらの州でのデング感染症の流行を防げる可能性はあります。
デング熱とデング出血熱の症例は、毎年米国へ帰国する旅行者に確認されています。
しかしながら、米国においてデングウイルス感染症について全国的に報告義務が課せられるようになったのは2009年の6月からで、2010年1月より前では症例報告が限られています。
熱帯地方のデング熱流行地からの帰国し、発熱の症状を示す旅行者の(血清診断による)感染率は3~8%に上ります。
GeoSentinel network(感染症に関するトラベルクリニックのネットワーク)のクリニックで診察を受けた罹病旅行者17,353人について最近実施された調査では、カリブ海地域、南米、南中央アジア、東南アジアからの帰国旅行者の全身性熱疾患の原因で最も多かったのはデング感染症であることを示しています。
また、熱帯地方からの帰国旅行者が入院治療を要するようになった原因で2番目に多いのはデング感染症(最も多い原因はマラリア)であるとする研究もあります。
デングウイルス感染によって生じる妊婦の健康状態や、母体のデングウイルス感染が発育中の胎児に与える影響について、公表されているデータは限られています。
母胎から胎児への垂直感染は起こりうることで、また周産期に母体が感染すると、新生児が症候性疾患を発症する可能性が高くなります。
文献で報告されている垂直感染の24症例では、発熱の母体発症と新生児発症の間には平均で7日(5~13日の範囲)の期間がありました。
すべての症例で発熱と血小板減少がみられ、また多くの症例で肝腫大と出血を認められました。
(以前の母体感染で生じた)母体の抗デングウイルスIgG抗体が胎盤を通して胎児に移行した場合には、生まれてくる新生児が生後6ヶ月から1歳になるまでの間にデングウイルスに感染すると、デング出血熱を発病するリスクが高くなります。
地図 3-01.デング熱流行地域(北中米カリブ海)
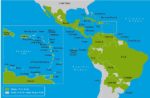
地図3-02.デング熱流行地域(アフリカ・中東)
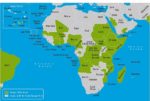
地図3-03.デング熱流行地域(アジア・オセアニア)
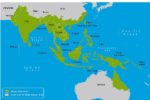
臨床症状
発熱があり、症状が現れる2週間前に熱帯地方や亜熱帯地方に旅行したことのある人の鑑別診断の際には、デング感染症であるか検討すべきです。
デング感染症の潜伏期は通常4~7日です(3~14日の範囲)。
デングウイルスに感染しても発熱が軽微な場合にはデング熱と診断されないかもしれません。
旅行者が初めてデングウイルスに感染しても、他の疾患との鑑別がつかない微熱性疾患に終わるか、あるいは症状が出ないことが多くあります。
しかし、その後にデングウイルスに再感染した場合、ふつうは重篤性の高い疾患になります。
WHOによる臨床上の定義では、デング熱は、頭痛、後眼窩痛、筋肉痛、関節痛、発疹、出血症状、白血球減少のうち2つ以上の症状が該当する急性熱疾患であるとしています。
発疹は通常発熱が治まるにつれて現れ、2~4日間持続します。斑状または斑状丘疹性の発疹で全身に広がり、正常皮膚の小斑と融合する場合が多くあり、落屑状になり痒みが出るようになることもあります。
デング熱のその他の症状・徴候として、皮膚の紅潮(通常は疾患発症24~48時間後)、吐き気、嘔吐があげられます。
デング熱患者のおよそ1%がデング出血熱を発病します。
これは発熱が治まりかけた時点(通常は発熱後3~8日経ってから)で起こります。
別の型のデングウイルスによって再感染した場合には、病状がより重篤化することがふつうです。
血管透過性の亢進と血漿漏出がデング出血熱とデング熱とを鑑別する所見となります。
デング出血熱の特徴として、
(1)発熱が2~7日間続く、
(2)出血症状の所見、あるいは駆血帯試験の陽性所見、
(3)血小板減少症(100,000個/mm3以下)、
(4)血液濃縮を含む血漿漏出の所見(すなわち、ヘマトクリット値が年齢別の平均値より20%以上上昇、あるいは輸液後にヘマトクリット値がベースライン値よりも20%以上低下)、
(5)胸水、
(6)腹水、
(7)低タンパク血症、などがあげられます。
血小板減少症だけではデング出血熱の診断にはなりません。
デングショック症候群の定義は、デング出血熱の診断を満たす基準に加えて、血圧低下、脈圧の狭小化(20mmHg以下)、または循環血液量減少性ショックの所見のいずれかが認められることとされています。
診断
デング感染症の疑いがある症例については、同一血清標本に対して行われる次の検査所見の組合せによって確定します。
(1)デングウイルスのゲノム配列またはデングウイルス抗原の検出(非構造蛋白1[NS1]抗原)、
(2)抗デングウイルスIgM抗体の血清診断。デングウイルスのゲノム配列またはNS1抗原の検出は、主に急性発熱期(発症後5日以内)に行われ、抗デングウイルスIgM抗体の検査は主に発熱して5日間が経過してから行われます。
血清、脳脊髄液、剖検組織の標本の細胞培養によってデング熱ウイルスを分離することはできますが、分子生物学的診断法の時代にあっては、とりわけ有用というものではありません。
血清あるいは血漿、脳脊髄液、剖検組織の標本からの特定のデング熱ウイルスゲノムの同定は、逆転写ポリメラーゼ連鎖反応法(RT-PCR)を用いてルーチンの検査として行うことができます。
NS1抗原はウイルス血症の期間に循環血中に見い出され、これを検出する何種類かの免疫学的測定法があります。
組織標本からのデング熱ウイルス抗原の同定は免疫蛍光測定法または免疫組織化学的分析法を用いて行うことができます。
急性患者のデング熱ウイルスの血清学的診断は、主として抗デングウイルスIgM抗体を対象とします。
この抗体はデング熱を発症してから5日過ぎてから陽性となります。
そのほか診断確定のための方法として次の検査所見があります。
(1) 急性期(発熱後5日以内)標本と回復期(発熱後5日経過の後)標本の間で、抗デングウイルスIgM抗体陽性転化のセロコンバージョン
(2) 回復期標本では急性期標本に対し、抗デングウイルス抗原に対する抗デングウイルスIgG抗体価または赤血球凝集抑制力価が4倍以上も上昇
(3) 脳脊髄液に抗デングウイルスIgM抗体
旅行歴や症状からデングウイルス感染の疑いがある場合に、単一血清標本で抗デングウイルスIgM抗体が検出されると、それはデングウイルス感染が最近になって起きた可能性を示唆しています。
しかし、単一標本で抗デングウイルスIgG抗体が検出されても、それがずっと以前の感染である可能性もあります。
単一標本を用いた抗体検査(抗デングウイルスIgMまたはIgG抗体)のみで診断を行うには注意が必要です。
なぜならデング熱ウイルス抗体は、西ナイル熱、黄熱病、日本脳炎ウイルスなどの他のフラビウイルスの抗体と交叉反応を起こすからです。
このため、他の種類のフラビウイルスとの感染があった場合あるいはそのウイルスのワクチン接種を行った場合には、抗デングウイルスIgMまたはIgG抗体検査が偽陽性の結果を示すことがあります。
市販されているデング熱を診断するための検査キットがいくつかありますが、いずれも米国食品医薬品局(Food and Drug Administration)の承認を受けたものではありません。
検査は米国疾病対策センター(CDC)でも行っています(検査依頼手続きについては、 www.cdc.gov/Dengue/clinicalLab/index.htmlの“Requesting Dengue Laboratory Testing and Reporting” を参照)。
急性期と回復期の血清標本を、州・準州の保健局の検査機関を通じてCDC(住所:1324 Calle Cañada, San Juan, Puerto Rico 00920-3860)へ送ります。
血清標本には、発症日、標本採取日、患者の最近の詳細な旅行歴などの臨床・疫学情報を記載した書類を添付する必要があります。
デング感染症についてさらに説明が必要な場合は、CDC Dengue Branch (787-706-2399)に問い合わせるか、ウェブサイトwww.cdc.gov/dengueを参照してください。
治療
デングウイルス感染症に対して特異的な治療法はありません。
発熱の間は、安静を保ち、脱水を防ぐために水分補給をするようにします。
解熱薬としてアセトアミノフェンを投与します。
頭痛、眼痛、関節痛、筋肉痛には麻薬の投与が必要になるかもしれません。
アスピリン剤、アスピリン配合薬、(イブプロフェンなどの)非ステロイド性抗炎症薬には抗凝固作用があるため、投与は避けるべきです。
アスピリンなどのサリチル酸塩は、ライ症侯群を併発する危険性があることから、小児への投与は特に避けなければなりません。
患者には熱が下がったときにデング出血熱またはデングショック症候群の前兆がないか注意を求め、次のような前兆が見られる場合には病院へ行くように指示します。
(1)発熱から低体温への急激な変化、
(2)激しい腹痛、
(3)嘔吐の持続、
(4)出血、
(5)呼吸困難、または(6)精神状態の悪化(興奮性、錯乱、無気力など)。
デング熱またはデングショック症候群の患者には、等張晶質液とコロイド液の静注輸液を速やかに適切に行うと転帰の改善につながります。
デング熱またはデングショック症候群では患者を入院させて、対症療法を施すとともに、バイタルサイン、体液バランス、血液パラメータ(ヘマトクリット値、血小板数)を厳重にモニターリングする必要があります。
予防措置
デング熱には感染予防のためのワクチンも薬剤もありません。
ウイルス保有の蚊に刺されると感染する恐れがあります。
蚊に刺されるリスクは、早朝、夜明けから数時間の間、夕方から日没にかけての時間に最も高くなります。
しかし、日中であればいつでも蚊は刺すものと思って間違いありません。
ネッタイシマカは通常屋内に生息し、大抵は戸棚、ベッドの下、カーテンの裏、浴室などの暗くて涼しい場所に潜んでいます。
旅行者は殺虫剤を散布してこうした場所にいる蚊を駆除するとともに、可能であれば、網戸が完備した窓やエアコンの設備がある宿泊施設を選ぶようにすべきです。
さらに旅行者自身も蚊に刺されないような対策を取る必要があります(Chapter 2 Protection against Mosquitos, Ticks and Other Arthropodsを参照)。
長期旅行者や国外居住者の場合は、さらに予防措置を講じて、宿泊施設の周囲にある(貯水槽や植木鉢のトレイなど)水が溜まる場所では水を抜いたり、消毒したり、容器に蓋をしたりします。
















